# 이 장에서 사용하는 패키지
library(tidyverse) # dplyr, tidyr, ggplot2, stringr, readr 등
library(lubridate) # 날짜/시간 처리
library(gt) # 출판 품질 테이블12 PK-PD 통합 데이터셋 구축
이 장에서는 약동학(PK) 데이터와 약력학(PD) 데이터를 하나의 통합 데이터셋(integrated PK-PD dataset)으로 구축하는 방법을 학습합니다. PK만 다루는 데이터셋과 달리, PK-PD 데이터셋은 약물 농도와 효과 지표를 동시에 포함해야 하므로 데이터 구조가 더 복잡합니다.
이 장의 실습 예제에서는 아토피 피부염(atopic dermatitis) 치료에 사용되는 JAK 억제제 Tofacitinib의 임상시험 데이터를 활용합니다. PK(혈중 농도)와 PD(SCORAD score)를 하나의 분석용 데이터셋으로 통합하는 전 과정을 다룹니다.
12.1 PK-PD 데이터셋 구조
12.1.1 PK 전용 데이터셋과의 차이점
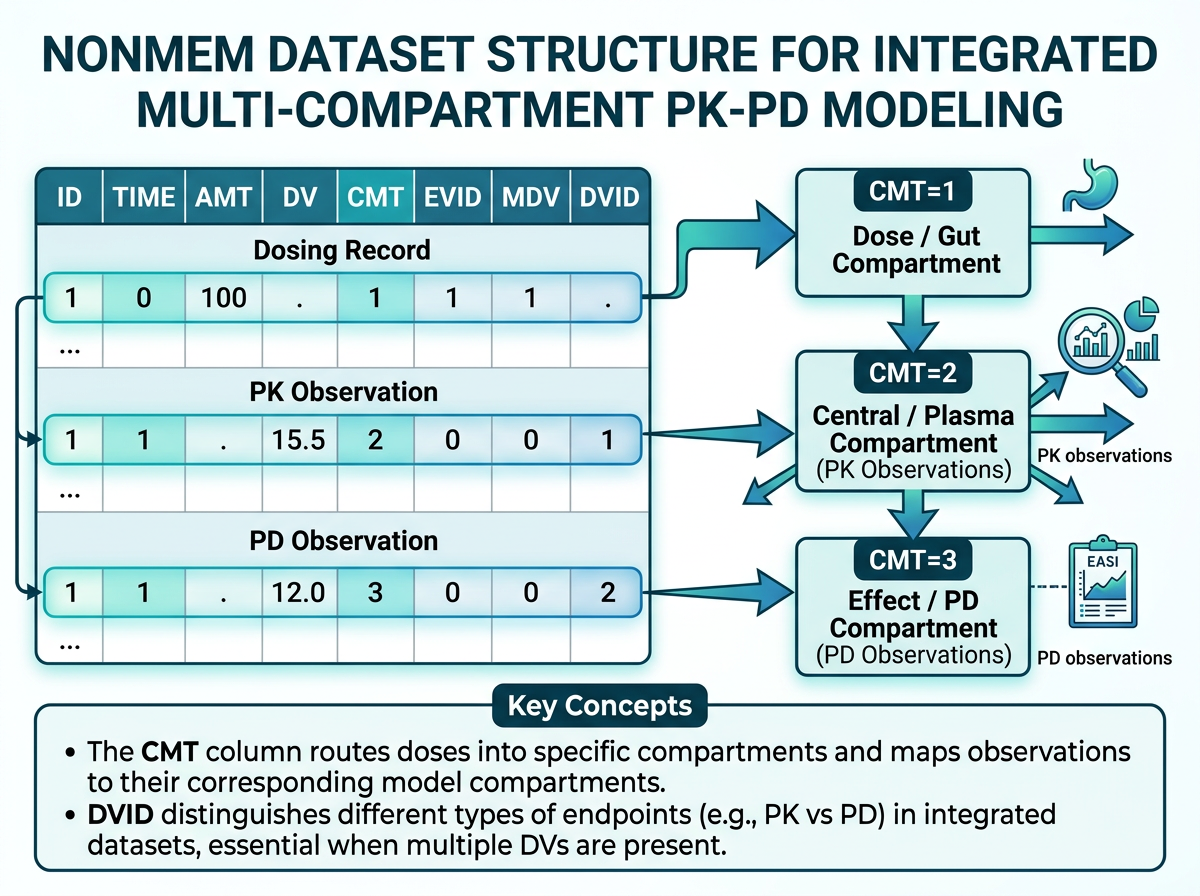
그림 12.1 은 PK-PD 통합 데이터셋의 다중 구획 구조와 EVID/MDV/DVID 매핑 관계를 보여줍니다. 지금까지 학습한 NONMEM 데이터셋은 PK 관측(약물 농도)만을 다뤘습니다. PK-PD 통합 데이터셋에서는 여기에 PD 관측(효과 지표)이 추가됩니다. 이로 인해 다음과 같은 구조적 변화가 필요합니다:
- CMT(Compartment)의 확장: PK 관측과 PD 관측이 서로 다른 구획에 속합니다
- DV(Dependent Variable)의 다중성: DV에 ng/mL 단위의 농도와 점수 단위의 SCORAD가 혼재합니다
- 시간 정렬(Time Alignment): PK와 PD 측정 시점이 대부분 다릅니다
- 추가 공변량: PD 분석에 필요한 시간 변동 공변량이 추가됩니다
12.1.2 Multiple CMT 체계
PK-PD 통합 데이터셋에서 CMT(Compartment) 번호는 레코드의 종류를 구분하는 핵심 역할을 합니다:
| CMT | 레코드 유형 | 설명 | EVID | MDV |
|---|---|---|---|---|
| 1 | 투약 (Dosing) | 약물 투여 기록 | 1 | 1 |
| 2 | PK 관측 (PK Observation) | 약물 농도 측정 | 0 | 0 |
| 3 | PD 관측 (PD Observation) | 효과 지표 측정 | 0 | 0 |
예를 들어, Tofacitinib을 투약하고 혈중 농도와 SCORAD score를 측정한 경우:
ID TIME DV AMT CMT EVID MDV DVID
1 0 . 5 1 1 1 .
1 0.5 125.3 0 2 0 0 1
1 1.0 310.8 0 2 0 0 1
1 0 62.5 0 3 0 0 2
1 336 45.2 0 3 0 0 2여기서 CMT=1은 투약, CMT=2는 PK 관측(혈중 농도), CMT=3은 PD 관측(SCORAD score)입니다.
12.1.3 DVID (Dependent Variable ID) 활용
DVID는 DV 컬럼에 저장된 값의 종류를 식별하는 변수입니다. PK-PD 데이터셋에서 DV에는 서로 다른 단위와 스케일의 값이 혼재하므로, DVID를 통해 이를 구분합니다:
| DVID | DV의 의미 | 단위 | 스케일 |
|---|---|---|---|
| 1 | 약물 농도 (PK) | ng/mL | 연속, 양수 |
| 2 | SCORAD score (PD) | 점 (0-103) | 연속, 양수 |
CMT와 DVID는 밀접하게 연관되어 있지만 동일하지 않습니다:
- CMT는 NONMEM 모델에서 구획을 지정하며, 투약 레코드(EVID=1)에도 사용됩니다
- DVID는 관측 레코드(EVID=0)에서 DV의 종류를 식별합니다
- 투약 레코드에서 DVID는 보통 결측(
.)이거나 0입니다 - PK 관측: CMT=2, DVID=1
- PD 관측: CMT=3, DVID=2
일부 모델링 소프트웨어(예: Monolix)에서는 DVID만으로 관측 유형을 구분하기도 합니다. NONMEM에서는 CMT와 DVID를 모두 사용하는 것이 일반적입니다.
12.1.4 시간 정렬 (Time Alignment) 전략
PK와 PD 측정 시점이 다를 때, 데이터를 하나의 타임라인에 배치해야 합니다. 이 과정을 시간 정렬(time alignment)이라고 합니다.
사례: Tofacitinib 아토피 피부염 시험
- PK 채혈: 투약 후 0, 0.5, 1, 2, 4, 8시간 (sparse sampling, 특정 방문일)
- PD 평가(SCORAD): Baseline(0주), 2주, 4주, 8주, 12주
이 경우 PK는 시간(hour) 단위로, PD는 주(week) 단위로 측정됩니다. 통합 데이터셋에서는 동일한 TIME 변수(보통 시간 단위)를 사용해야 합니다:
- PD 관측의 TIME은 방문일을 시간으로 변환합니다: 2주 = 336시간, 4주 = 672시간 등
- 같은 방문일에 PK와 PD가 모두 측정된 경우, 투약 → PK 관측 → PD 관측 순서로 정렬합니다
# 시간 변환 예시: 주 → 시간
visit_weeks <- c(0, 2, 4, 8, 12)
visit_hours <- visit_weeks * 7 * 24 # 주 × 7일 × 24시간
tibble(
Visit_Week = visit_weeks,
Visit_Hour = visit_hours,
Visit_Label = paste0("Week ", visit_weeks)
)TIME 변수의 기준점(시간 0)은 일반적으로 첫 번째 투약 시점으로 설정합니다. PD 데이터에서 baseline 측정이 투약 전에 이루어진 경우:
- Baseline PD 관측: TIME = 0 (또는 투약 직전의 음수 시간)
- 첫 투약: TIME = 0
- 이후 PD 관측: TIME = 해당 방문의 시간(시간 단위)
Baseline PD와 첫 투약의 TIME이 모두 0인 경우, EVID와 CMT의 조합으로 구분할 수 있지만, 데이터 정렬에 주의가 필요합니다. 실무에서는 baseline PD를 TIME = -0.01 등으로 약간 앞에 배치하는 경우도 있습니다.
12.2 NONMEM PK-PD 데이터셋 확장
12.2.1 CMT, EVID, MDV 확장 규칙
PK 전용 데이터셋에서 PK-PD 데이터셋으로 확장할 때, 각 필수 컬럼의 규칙을 명확히 이해해야 합니다.
확장된 레코드 유형과 컬럼 값:
| 레코드 유형 | CMT | EVID | MDV | AMT | DV | DVID |
|---|---|---|---|---|---|---|
| 경구 투약 | 1 | 1 | 1 | 투여량(mg) | 0 또는 . |
0 또는 . |
| PK 관측 (정량 가능) | 2 | 0 | 0 | 0 | 농도(ng/mL) | 1 |
| PK 관측 (BLQ) | 2 | 0 | 1 | 0 | 0 | 1 |
| PD 관측 (SCORAD) | 3 | 0 | 0 | 0 | SCORAD | 2 |
| PD 관측 (결측) | 3 | 0 | 1 | 0 | . |
2 |
PD 관측에서 MDV를 잘못 설정하는 것은 PK-PD 데이터셋에서 가장 흔한 오류 중 하나입니다:
- PD 값이 존재하면 MDV = 0 (NONMEM이 이 값을 fitting에 사용)
- PD 값이 결측이면 MDV = 1 (NONMEM이 이 행의 DV를 무시)
- PD 값이 0인 경우(예: SCORAD = 0): MDV = 0 (0은 유효한 관측값)
- PD baseline 관측: MDV = 0 (baseline도 유효한 관측값)
MDV=1로 설정하면 해당 레코드는 모델 추정에 기여하지 않으므로, 의도치 않게 데이터를 잃을 수 있습니다.
12.2.2 DV 스케일링: PK와 PD 단위 차이 처리
PK-PD 데이터셋에서 가장 중요한 고려사항 중 하나는 DV의 스케일 차이입니다:
- PK (약물 농도): 1~1,000 ng/mL 범위
- PD (SCORAD score): 0~103 범위
이 스케일 차이를 처리하는 방법은 크게 세 가지입니다:
방법 1: DVID 기반 분리
NONMEM 모델 코드에서 DVID를 사용하여 PK와 PD의 잔차 오차를 별도로 정의합니다. 이 경우 DV를 별도로 스케일링할 필요가 없습니다.
# DV는 원래 단위 그대로 유지
pk_pd_data <- tibble(
ID = 1,
TIME = c(0, 0.5, 1, 336),
DV = c(NA, 125.3, 310.8, 45.2), # ng/mL과 SCORAD 혼재
CMT = c(1, 2, 2, 3),
EVID = c(1, 0, 0, 0),
MDV = c(1, 0, 0, 0),
DVID = c(NA, 1, 1, 2)
)방법 2: 로그 변환
PK 데이터를 로그 변환하여 사용하는 경우, PD 데이터도 로그 변환할 수 있습니다. 단, PD 데이터의 특성에 따라 로그 변환이 적절하지 않을 수 있습니다.
# 로그 변환 적용 예시
pk_pd_data <- pk_pd_data |>
mutate(
# LDV: 로그 변환된 DV
LDV = case_when(
EVID == 1 ~ NA_real_, # 투약 레코드
DVID == 1 & DV > 0 ~ log(DV), # PK: 자연로그
DVID == 2 & DV > 0 ~ log(DV), # PD: 자연로그 (적절한 경우)
TRUE ~ NA_real_
)
)방법 3: 표준화/정규화
PD 데이터를 baseline 대비 변화율로 변환하여 스케일을 조정합니다.
# PD 데이터를 baseline 대비 변화로 변환
pd_data <- pd_data |>
group_by(ID) |>
mutate(
SCORAD_BL = first(SCORAD), # baseline SCORAD
SCORAD_CFB = SCORAD - SCORAD_BL, # change from baseline (절대)
SCORAD_PCFB = (SCORAD - SCORAD_BL) / SCORAD_BL * 100 # percent change from baseline
) |>
ungroup()12.2.3 여러 PD 엔드포인트 동시 포함
실제 임상시험에서는 여러 PD 엔드포인트를 동시에 분석하는 경우가 있습니다. 예를 들어 아토피 피부염 시험에서:
| DVID | 엔드포인트 | CMT | 단위 |
|---|---|---|---|
| 1 | Tofacitinib 농도 | 2 | ng/mL |
| 2 | SCORAD score | 3 | 점 (0-103) |
| 3 | 림프구 수 (ALC) | 4 | cells/μL |
| 4 | 가려움증 NRS | 5 | 점 (0-10) |
# 다중 PD 엔드포인트 데이터셋 구조 예시
multi_pd <- tribble(
~ID, ~TIME, ~DV, ~CMT, ~EVID, ~MDV, ~DVID, ~ENDPOINT,
1, 0, NA, 1, 1, 1, NA, "DOSE",
1, 0.5, 125.3, 2, 0, 0, 1, "PK",
1, 0, 62.5, 3, 0, 0, 2, "SCORAD",
1, 0, 1850, 4, 0, 0, 3, "ALC",
1, 0, 7.2, 5, 0, 0, 4, "NRS",
1, 336, 45.2, 3, 0, 0, 2, "SCORAD",
1, 336, 1420, 4, 0, 0, 3, "ALC",
1, 336, 4.1, 5, 0, 0, 4, "NRS"
)- DVID와 CMT의 매핑 테이블을 반드시 문서화하세요
- 각 엔드포인트의 단위, 정상 범위, 임상적 의미를 기록하세요
- 모델링 소프트웨어에 따라 지원하는 DVID 수에 제한이 있을 수 있습니다
- DV 스케일이 극단적으로 다른 경우 (예: ng/mL vs cells/μL), 모델 수렴에 문제가 생길 수 있으므로 적절한 스케일링이 필요합니다
12.3 공변량 데이터 통합
12.3.1 시간 변동 공변량 (Time-Varying Covariates)
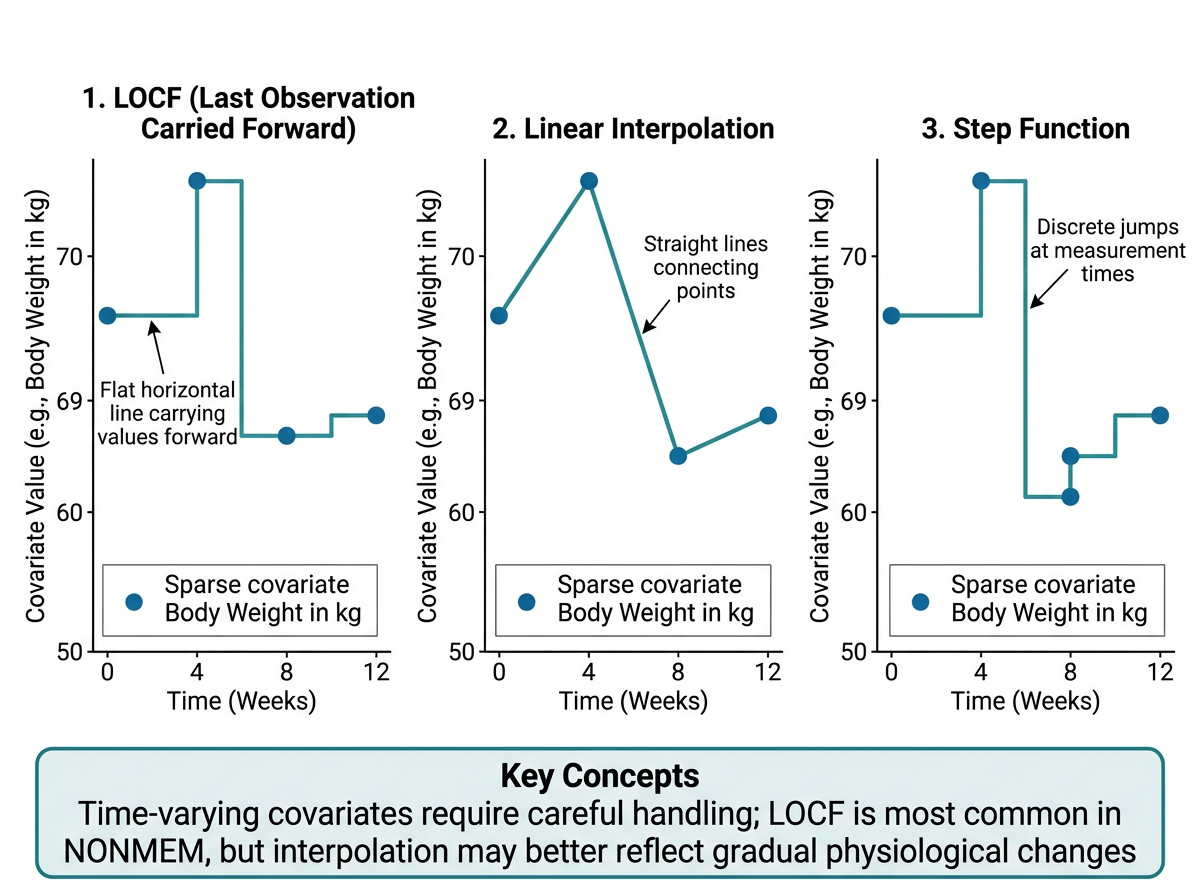
그림 12.2 는 세 가지 시간변동 공변량 처리 방법(LOCF, 선형 보간, 계단 함수)을 비교한 것입니다. PK-PD 분석에서는 시간에 따라 변하는 공변량이 중요한 역할을 합니다. 아토피 피부염 치료에서의 대표적인 시간 변동 공변량:
| 공변량 | 측정 빈도 | 임상적 의미 |
|---|---|---|
| 체중 (WT) | 매 방문 | 약물 청소율에 영향 |
| 림프구 수 (ALC) | 2-4주마다 | JAK 억제제의 면역 억제 효과 모니터링 |
| 알부민 (ALB) | 4주마다 | 약물 결합/분포에 영향 |
| 크레아티닌 청소율 (CrCL) | 4-8주마다 | 신장 배설에 영향 |
| 간 효소 (ALT, AST) | 2-4주마다 | 간독성 모니터링 |
시간 변동 공변량은 NONMEM 데이터셋에서 측정 시점에 해당하는 행에 값을 기록합니다. 측정되지 않은 시점에서는 이전 값을 이월하거나(LOCF) 보간합니다.
# 시간 변동 공변량 데이터 예시
tv_covariates <- tribble(
~ID, ~VISIT_WEEK, ~WT, ~ALC, ~ALB,
1, 0, 68.5, 1850, 4.2,
1, 2, 68.2, 1620, 4.1,
1, 4, 67.8, 1420, 4.0,
1, 8, 67.5, 1380, 3.9,
1, 12, 67.2, 1350, 4.0,
2, 0, 55.0, 2100, 4.5,
2, 2, 54.8, 1780, 4.4,
2, 4, 54.5, 1550, 4.3,
2, 8, 54.2, 1520, 4.2,
2, 12, 54.0, 1510, 4.3
)12.3.2 기저치 공변량 (Baseline Covariates)
기저치 공변량은 연구 시작 시점에 한 번 측정되며 시간에 따라 변하지 않는 것으로 가정합니다:
| 공변량 | 데이터셋에서의 표현 |
|---|---|
| 나이 (AGE) | 모든 레코드에 동일한 값 |
| 성별 (SEX) | 0=남, 1=여 (또는 반대) |
| 인종 (RACE) | 숫자 코딩 (1=아시아인, 2=백인 등) |
| Baseline SCORAD (BSCRD) | Screening 또는 Day 1의 SCORAD |
| Baseline 체중 (BWT) | Day 1의 체중 |
| CYP3A4/2C19 유전자형 | 약물 대사 관련 |
# 기저치 공변량 데이터
baseline_cov <- tribble(
~ID, ~AGE, ~SEX, ~RACE, ~BWT, ~BSCRD, ~CYP3A4,
1, 34, 0, 1, 68.5, 62.5, "EM",
2, 28, 1, 1, 55.0, 71.0, "EM",
3, 45, 0, 2, 82.0, 58.3, "PM",
4, 39, 1, 1, 61.0, 65.8, "IM",
5, 52, 0, 1, 75.5, 74.2, "EM",
6, 31, 1, 2, 58.0, 60.1, "EM"
)12.3.3 LOCF vs 보간 (Interpolation)
시간 변동 공변량이 측정되지 않은 시점에서 값을 할당하는 두 가지 방법:
LOCF (Last Observation Carried Forward)
가장 최근에 측정된 값을 다음 측정 시점까지 이월합니다. 가장 일반적으로 사용되는 방법입니다.
# LOCF 구현
pk_pd_with_cov <- pk_pd_data |>
left_join(tv_covariates, by = c("ID", "VISIT_WEEK")) |>
group_by(ID) |>
arrange(ID, TIME) |>
fill(WT, ALC, ALB, .direction = "down") |> # LOCF: 아래로 채우기
ungroup()선형 보간 (Linear Interpolation)
두 측정 시점 사이의 값을 선형으로 추정합니다. 체중과 같이 연속적으로 변하는 공변량에 적합합니다.
# 선형 보간 구현
library(zoo) # na.approx 함수 사용
pk_pd_interpolated <- pk_pd_data |>
group_by(ID) |>
arrange(ID, TIME) |>
mutate(
WT_interp = zoo::na.approx(WT, TIME, na.rm = FALSE),
ALC_interp = zoo::na.approx(ALC, TIME, na.rm = FALSE),
ALB_interp = zoo::na.approx(ALB, TIME, na.rm = FALSE)
) |>
ungroup()| 상황 | 권장 방법 | 이유 |
|---|---|---|
| 체중 | LOCF 또는 보간 | 서서히 변하므로 큰 차이 없음 |
| 림프구 수 | LOCF | 약물 효과로 급격히 변할 수 있어 보간이 부정확할 수 있음 |
| 알부민 | LOCF | 측정 빈도가 낮고 변화폭이 작음 |
| 크레아티닌 | LOCF | 급격한 변화 시 보간이 적절하지 않음 |
대부분의 집단약동학 분석에서는 LOCF가 표준입니다. FDA 가이던스에서도 LOCF를 기본 방법으로 권장합니다.
12.3.4 데이터 매핑 문서 (Data Specification) 작성
PK-PD 데이터셋의 모든 변수를 문서화하는 데이터 사양서(Data Specification)는 필수입니다. 이 문서는 규제기관 제출 시 분석 계획과 함께 제출됩니다.
# 데이터 사양서 자동 생성 함수
create_data_spec <- function(data, dataset_name = "PK-PD Dataset") {
spec <- tibble(
Variable = names(data),
Type = map_chr(data, ~ class(.x)[1]),
N_Unique = map_int(data, n_distinct),
N_Missing = map_int(data, ~ sum(is.na(.x))),
Pct_Missing = round(N_Missing / nrow(data) * 100, 1),
Min = map_chr(data, ~ if (is.numeric(.x)) as.character(round(min(.x, na.rm = TRUE), 3)) else NA_character_),
Max = map_chr(data, ~ if (is.numeric(.x)) as.character(round(max(.x, na.rm = TRUE), 3)) else NA_character_),
Example = map_chr(data, ~ as.character(.x[!is.na(.x)][1]))
)
spec |>
gt() |>
tab_header(
title = paste("Data Specification:", dataset_name),
subtitle = paste("N rows:", nrow(data), "| N columns:", ncol(data))
) |>
fmt_number(columns = Pct_Missing, decimals = 1) |>
cols_label(
Variable = "변수명",
Type = "데이터 유형",
N_Unique = "고유값 수",
N_Missing = "결측 수",
Pct_Missing = "결측률(%)",
Min = "최소값",
Max = "최대값",
Example = "예시 값"
)
}
# 사용 예시
# create_data_spec(pk_pd_final, "Tofacitinib PK-PD Integrated Dataset")12.4 R 실습: Tofacitinib PK + SCORAD 통합
12.4.1 시험 설계 개요
이 실습에서는 다음과 같은 가상의 임상시험 시나리오를 사용합니다:
- 시험명: Tofacitinib Phase II Dose-Finding Study in Atopic Dermatitis
- 대상: 중등도-중증 아토피 피부염 성인 환자 60명
- 용량군: Tofacitinib 5mg BID (30명) vs 10mg BID (30명)
- 치료 기간: 12주
- PK 채혈: Day 1, Week 4, Week 12에 sparse sampling (투약 후 1, 2, 4시간)
- PD 평가: SCORAD score (baseline, Week 2, 4, 8, 12)
- 안전성: 림프구 수(ALC) 모니터링 (baseline, Week 2, 4, 8, 12)
- 분석법 LLOQ: 0.5 ng/mL
12.4.2 Step 1: 인구통계 데이터 생성
# Tofacitinib PK-PD 데이터를 CSV 파일에서 불러오기
tofa_pkpd <- read_csv("data/pkpd_tofacitinib.csv")
glimpse(tofa_pkpd)
# 이 데이터에는 이미 PK(CAVG)와 PD(SCORAD, LYMPHOCYTE)가 통합되어 있습니다
# 아래에서는 원시 데이터 → NONMEM 형식 구축 과정을 시연합니다
set.seed(12345)
n_subjects <- 60
# 인구통계 데이터
demo <- tibble(
ID = 1:n_subjects,
AGE = round(rnorm(n_subjects, mean = 38, sd = 12)),
SEX = sample(c(0, 1), n_subjects, replace = TRUE, prob = c(0.45, 0.55)),
RACE = sample(c(1, 2, 3), n_subjects, replace = TRUE, prob = c(0.6, 0.3, 0.1)),
BWT = round(rnorm(n_subjects, mean = 67, sd = 12), 1),
HT = round(rnorm(n_subjects, mean = 168, sd = 9), 1),
DOSE_GRP = rep(c(5, 10), each = 30),
BSCRD = round(rnorm(n_subjects, mean = 65, sd = 10), 1) # baseline SCORAD
) |>
mutate(
AGE = pmax(AGE, 18) |> pmin(75), # 18-75세 범위
BWT = pmax(BWT, 40) |> pmin(120),
BSCRD = pmax(BSCRD, 40) |> pmin(90), # 중등도-중증 범위
BMI = round(BWT / (HT / 100)^2, 1),
BSA = round(0.007184 * BWT^0.425 * HT^0.725, 2), # DuBois 공식
# CYP2C19 유전자형 (대사 표현형)
CYP2C19 = sample(c(1, 2, 3), n_subjects, replace = TRUE, prob = c(0.6, 0.3, 0.1))
# 1 = EM, 2 = IM, 3 = PM
)
demo |> head(10)12.4.3 Step 2: 투약 데이터 생성
# 12주 BID 투약 스케줄 생성
# BID: 1일 2회 (아침 8시, 저녁 8시) → 12시간 간격
create_dosing_records <- function(id, dose, duration_weeks = 12) {
n_days <- duration_weeks * 7
n_doses <- n_days * 2 # BID
tibble(
ID = id,
TIME = seq(0, by = 12, length.out = n_doses), # 12시간 간격
DV = NA_real_,
AMT = dose,
CMT = 1,
EVID = 1,
MDV = 1,
DVID = NA_real_
)
}
# 모든 대상자의 투약 데이터
dosing_data <- map2_dfr(
demo$ID,
demo$DOSE_GRP,
~ create_dosing_records(.x, .y)
)
# 투약 레코드 수 확인
dosing_data |>
group_by(ID) |>
summarise(n_doses = n(), total_amt = sum(AMT)) |>
head()12.4.4 Step 3: PK 데이터 생성
# Tofacitinib PK: 1-구획 모델 기반 시뮬레이션 (단순화)
# CL/F = 30 L/hr, V/F = 100 L, ka = 2 hr^-1, F = 0.74
simulate_pk <- function(id, dose, demo_data, pk_times, pk_days) {
subj <- demo_data |> filter(ID == id)
# 개인 간 변동 (IIV)
eta_cl <- rnorm(1, 0, 0.3) # 30% CV
eta_v <- rnorm(1, 0, 0.2) # 20% CV
# 공변량 효과 (체중)
CL <- 30 * (subj$BWT / 70)^0.75 * exp(eta_cl) # L/hr
V <- 100 * (subj$BWT / 70) * exp(eta_v) # L
ka <- 2 # hr^-1
ke <- CL / V
# CYP2C19 효과
if (subj$CYP2C19 == 2) CL <- CL * 0.75 # IM: CL 25% 감소
if (subj$CYP2C19 == 3) CL <- CL * 0.50 # PM: CL 50% 감소
records <- list()
for (day in pk_days) {
day_hours <- (day - 1) * 24
# 정상상태 근사: 투약 후 각 시점의 농도 계산
for (t_post_dose in pk_times) {
t_actual <- day_hours + t_post_dose
# 단순 1구획 경구 모델 (정상상태 근사)
conc <- (dose * 1000 / V) * (ka / (ka - ke)) *
(exp(-ke * t_post_dose) - exp(-ka * t_post_dose)) /
(1 - exp(-ke * 12)) # 12시간 간격 정상상태 보정
# 잔차 오차
conc <- conc * exp(rnorm(1, 0, 0.15)) # 비례 오차 15%
records[[length(records) + 1]] <- tibble(
ID = id,
TIME = t_actual,
DV = round(max(conc, 0), 2),
AMT = 0,
CMT = 2,
EVID = 0,
MDV = 0,
DVID = 1
)
}
}
bind_rows(records)
}
# PK 채혈 시점과 날짜
pk_sample_times <- c(1, 2, 4) # 투약 후 시간
pk_sample_days <- c(1, 28, 84) # Day 1, Week 4, Week 12
# 모든 대상자의 PK 데이터 시뮬레이션
pk_data <- map2_dfr(
demo$ID,
demo$DOSE_GRP,
~ simulate_pk(.x, .y, demo, pk_sample_times, pk_sample_days)
)
# BLQ 처리: LLOQ = 0.5 ng/mL
pk_data <- pk_data |>
mutate(
BLQ = if_else(DV < 0.5, 1, 0),
DV = if_else(BLQ == 1, 0, DV),
MDV = if_else(BLQ == 1, 1, 0)
)
pk_data |>
group_by(DVID) |>
summarise(
n_obs = n(),
n_blq = sum(BLQ),
pct_blq = round(mean(BLQ) * 100, 1),
mean_dv = round(mean(DV[DV > 0], na.rm = TRUE), 2),
.groups = "drop"
)12.4.5 Step 4: PD 데이터 생성
# SCORAD score 시뮬레이션
# 약물 효과: Emax 모델, SCORAD = baseline * (1 - Emax * Cavg / (EC50 + Cavg))
simulate_pd <- function(id, dose, demo_data, visit_weeks) {
subj <- demo_data |> filter(ID == id)
baseline_scorad <- subj$BSCRD
# 개인별 Emax, EC50의 변동
eta_emax <- rnorm(1, 0, 0.2)
eta_ec50 <- rnorm(1, 0, 0.3)
Emax <- 0.70 * exp(eta_emax) # 최대 70% 개선
EC50 <- 80 * exp(eta_ec50) # ng/mL (Cavg 기준)
# 대략적인 정상상태 Cavg 추정 (dose * F / (CL * tau))
CL_approx <- 30 * (subj$BWT / 70)^0.75
Cavg <- (dose * 1000 * 0.74) / (CL_approx * 12) # ng/mL
records <- list()
for (week in visit_weeks) {
time_hours <- week * 7 * 24
if (week == 0) {
scorad <- baseline_scorad
} else {
# 시간 의존 효과 (점진적 효과 발현)
time_effect <- 1 - exp(-week / 4) # ~4주에 63% 효과 발현
effect <- Emax * Cavg / (EC50 + Cavg) * time_effect
scorad <- baseline_scorad * (1 - effect) + rnorm(1, 0, 3) # 잔차
scorad <- max(scorad, 0) |> min(103) # SCORAD 범위: 0-103
}
records[[length(records) + 1]] <- tibble(
ID = id,
TIME = time_hours,
DV = round(scorad, 1),
AMT = 0,
CMT = 3,
EVID = 0,
MDV = 0,
DVID = 2
)
}
bind_rows(records)
}
# PD 방문 시점
pd_visit_weeks <- c(0, 2, 4, 8, 12)
# 모든 대상자의 PD 데이터 시뮬레이션
pd_data <- map2_dfr(
demo$ID,
demo$DOSE_GRP,
~ simulate_pd(.x, .y, demo, pd_visit_weeks)
)
pd_data |>
group_by(DVID, TIME) |>
summarise(
n = n(),
mean = round(mean(DV), 1),
sd = round(sd(DV), 1),
.groups = "drop"
)12.4.6 Step 5: 시간 변동 공변량 (림프구 수) 데이터
# 림프구 수 (ALC) 시뮬레이션
# Tofacitinib은 용량 의존적으로 림프구를 감소시킴
simulate_alc <- function(id, dose, demo_data, visit_weeks) {
subj <- demo_data |> filter(ID == id)
# Baseline ALC: 정상 범위 1000-4800 cells/μL
baseline_alc <- rnorm(1, mean = 2200, sd = 500) |> max(1000)
eta_drug <- rnorm(1, 0, 0.2)
# 용량 의존적 감소: 5mg → ~15% 감소, 10mg → ~25% 감소
max_decrease <- (0.15 + 0.10 * (dose / 10)) * exp(eta_drug)
records <- list()
for (week in visit_weeks) {
time_hours <- week * 7 * 24
if (week == 0) {
alc <- baseline_alc
} else {
time_effect <- 1 - exp(-week / 3)
alc <- baseline_alc * (1 - max_decrease * time_effect) + rnorm(1, 0, 100)
alc <- max(alc, 200) # 최소값 제한
}
records[[length(records) + 1]] <- tibble(
ID = id,
VISIT_WEEK = week,
TIME = time_hours,
ALC = round(alc)
)
}
bind_rows(records)
}
# ALC 데이터 시뮬레이션
alc_data <- map2_dfr(
demo$ID,
demo$DOSE_GRP,
~ simulate_alc(.x, .y, demo, pd_visit_weeks)
)
alc_data |>
group_by(VISIT_WEEK) |>
summarise(
n = n(),
mean_alc = round(mean(ALC)),
sd_alc = round(sd(ALC)),
.groups = "drop"
)12.4.7 Step 6: PK + PD + 공변량 데이터 병합
# Step 6-1: 투약 + PK + PD 데이터 병합
pk_pd_combined <- bind_rows(
dosing_data,
pk_data |> select(ID, TIME, DV, AMT, CMT, EVID, MDV, DVID),
pd_data
) |>
arrange(ID, TIME, desc(EVID), CMT) |> # ID → TIME → 투약 먼저 → CMT 순서
mutate(
# 레코드 순서 번호
ROW = row_number()
)
# Step 6-2: 기저치 공변량 병합
pk_pd_with_baseline <- pk_pd_combined |>
left_join(
demo |> select(ID, AGE, SEX, RACE, BWT, HT, BMI, BSA, BSCRD, CYP2C19, DOSE_GRP),
by = "ID"
)
# Step 6-3: 시간 변동 공변량 (ALC) 병합 — LOCF 방법
# 먼저 ALC 데이터를 TIME 기반으로 병합
alc_for_merge <- alc_data |>
select(ID, TIME, ALC)
pk_pd_with_cov <- pk_pd_with_baseline |>
left_join(alc_for_merge, by = c("ID", "TIME")) |>
group_by(ID) |>
arrange(ID, TIME) |>
fill(ALC, .direction = "down") |> # LOCF
ungroup()
# Step 6-4: Baseline ALC 추가
baseline_alc <- alc_data |>
filter(VISIT_WEEK == 0) |>
select(ID, BALC = ALC)
pk_pd_final <- pk_pd_with_cov |>
left_join(baseline_alc, by = "ID")
pk_pd_final |>
head(20) |>
select(ID, TIME, DV, AMT, CMT, EVID, MDV, DVID, AGE, SEX, DOSE_GRP, ALC, BALC)12.4.8 Step 7: 데이터 검증
# PK-PD 데이터셋 검증 함수
validate_pkpd_dataset <- function(data) {
checks <- list()
# 1. 필수 컬럼 존재 확인
required_cols <- c("ID", "TIME", "DV", "AMT", "CMT", "EVID", "MDV", "DVID")
missing_cols <- setdiff(required_cols, names(data))
checks$required_columns <- tibble(
Check = "필수 컬럼 존재",
Status = if (length(missing_cols) == 0) "PASS" else "FAIL",
Detail = if (length(missing_cols) == 0) "모든 필수 컬럼 존재" else paste("누락:", paste(missing_cols, collapse = ", "))
)
# 2. EVID=1일 때 AMT > 0 확인
dose_check <- data |> filter(EVID == 1)
checks$dose_amt <- tibble(
Check = "투약 레코드 AMT > 0",
Status = if (all(dose_check$AMT > 0, na.rm = TRUE)) "PASS" else "FAIL",
Detail = paste("투약 레코드", nrow(dose_check), "개 중 AMT ≤ 0:", sum(dose_check$AMT <= 0, na.rm = TRUE), "개")
)
# 3. EVID=1일 때 MDV=1 확인
checks$dose_mdv <- tibble(
Check = "투약 레코드 MDV=1",
Status = if (all(dose_check$MDV == 1)) "PASS" else "FAIL",
Detail = paste("MDV ≠ 1인 투약 레코드:", sum(dose_check$MDV != 1), "개")
)
# 4. 관측 레코드에서 MDV=0이면 DV 유효 확인
obs_check <- data |> filter(EVID == 0, MDV == 0)
checks$obs_dv <- tibble(
Check = "관측 레코드 DV 유효성",
Status = if (all(!is.na(obs_check$DV))) "PASS" else "WARNING",
Detail = paste("MDV=0인 관측 레코드 중 DV 결측:", sum(is.na(obs_check$DV)), "개")
)
# 5. 각 ID별 TIME 단조 증가 확인 (동일 TIME 허용)
time_check <- data |>
group_by(ID) |>
summarise(monotonic = all(diff(TIME) >= 0), .groups = "drop")
checks$time_order <- tibble(
Check = "TIME 단조 증가",
Status = if (all(time_check$monotonic)) "PASS" else "FAIL",
Detail = paste("TIME 역전 대상자:", sum(!time_check$monotonic), "명")
)
# 6. CMT-DVID 일관성 확인
obs_data <- data |> filter(EVID == 0)
cmt_dvid_check <- obs_data |>
filter(
(CMT == 2 & DVID != 1) |
(CMT == 3 & DVID != 2)
)
checks$cmt_dvid <- tibble(
Check = "CMT-DVID 일관성",
Status = if (nrow(cmt_dvid_check) == 0) "PASS" else "FAIL",
Detail = paste("불일치 레코드:", nrow(cmt_dvid_check), "개")
)
# 7. 각 ID에 투약 레코드 존재 확인
ids_with_dose <- data |> filter(EVID == 1) |> pull(ID) |> unique()
ids_without_dose <- setdiff(unique(data$ID), ids_with_dose)
checks$dose_exists <- tibble(
Check = "모든 ID에 투약 레코드 존재",
Status = if (length(ids_without_dose) == 0) "PASS" else "FAIL",
Detail = paste("투약 레코드 없는 ID:", length(ids_without_dose), "개")
)
# 8. 각 ID에 PK와 PD 관측 레코드 존재 확인
pk_ids <- data |> filter(DVID == 1) |> pull(ID) |> unique()
pd_ids <- data |> filter(DVID == 2) |> pull(ID) |> unique()
checks$obs_exists <- tibble(
Check = "PK/PD 관측 레코드 존재",
Status = if (length(setdiff(unique(data$ID), pk_ids)) == 0 &
length(setdiff(unique(data$ID), pd_ids)) == 0) "PASS" else "WARNING",
Detail = paste("PK 관측 없는 ID:", length(setdiff(unique(data$ID), pk_ids)),
"| PD 관측 없는 ID:", length(setdiff(unique(data$ID), pd_ids)))
)
# 결과 요약
result <- bind_rows(checks)
return(result)
}
# 검증 실행
validation_result <- validate_pkpd_dataset(pk_pd_final)
validation_result |>
gt() |>
tab_header(title = "PK-PD 데이터셋 검증 결과") |>
tab_style(
style = cell_fill(color = "#d4edda"),
locations = cells_body(rows = Status == "PASS")
) |>
tab_style(
style = cell_fill(color = "#f8d7da"),
locations = cells_body(rows = Status == "FAIL")
) |>
tab_style(
style = cell_fill(color = "#fff3cd"),
locations = cells_body(rows = Status == "WARNING")
)12.4.9 Step 8: 중복 및 결측 확인
# 중복 레코드 확인
duplicates <- pk_pd_final |>
group_by(ID, TIME, CMT, EVID) |>
filter(n() > 1) |>
ungroup()
cat("중복 레코드 수:", nrow(duplicates), "\n")
# 결측 패턴 요약
missing_summary <- pk_pd_final |>
summarise(
across(everything(), ~ sum(is.na(.x)))
) |>
pivot_longer(everything(), names_to = "Variable", values_to = "N_Missing") |>
filter(N_Missing > 0) |>
arrange(desc(N_Missing))
missing_summary12.4.10 Step 9: 최종 데이터셋 내보내기 및 요약
# 최종 데이터셋 요약
cat("=== PK-PD 통합 데이터셋 요약 ===\n\n")
cat("총 레코드 수:", nrow(pk_pd_final), "\n")
cat("대상자 수:", n_distinct(pk_pd_final$ID), "\n\n")
pk_pd_final |>
group_by(Record_Type = case_when(
EVID == 1 ~ "투약 (EVID=1)",
DVID == 1 ~ "PK 관측 (DVID=1)",
DVID == 2 ~ "PD 관측 (DVID=2)",
TRUE ~ "기타"
)) |>
summarise(
N_Records = n(),
N_Subjects = n_distinct(ID),
.groups = "drop"
) |>
gt() |>
tab_header(title = "레코드 유형별 요약")
# CSV 내보내기
# 결측값을 '.'으로 변환 (NONMEM 형식)
pk_pd_export <- pk_pd_final |>
select(ID, TIME, DV, AMT, CMT, EVID, MDV, DVID,
AGE, SEX, RACE, BWT, HT, BMI, BSA,
DOSE_GRP, BSCRD, CYP2C19, ALC, BALC) |>
mutate(across(everything(), ~ if_else(is.na(.x), ".", as.character(.x))))
# write_csv(pk_pd_export, "tofacitinib_pkpd_dataset.csv", na = ".")12.4.11 Step 10: 데이터 사양서 생성
# 데이터 사양서 (Data Specification)
data_spec <- tribble(
~Variable, ~Label, ~Type, ~Unit, ~Values, ~Source,
"ID", "대상자 식별 번호", "Integer", "-", "1-60", "DM",
"TIME", "상대 시간 (첫 투약 기준)", "Numeric", "hour", "0-2016", "Derived",
"DV", "종속 변수", "Numeric", "ng/mL or score", "PK: 0.5-500, PD: 0-103", "PC/PD",
"AMT", "투약량", "Numeric", "mg", "5, 10", "EX",
"CMT", "구획 번호", "Integer", "-", "1=투약, 2=PK, 3=PD", "Derived",
"EVID", "이벤트 ID", "Integer", "-", "0=관측, 1=투약", "Derived",
"MDV", "Missing Dependent Variable", "Integer", "-", "0=있음, 1=없음", "Derived",
"DVID", "종속변수 ID", "Integer", "-", "1=PK, 2=PD", "Derived",
"AGE", "나이", "Numeric", "year", "18-75", "DM",
"SEX", "성별", "Integer", "-", "0=남, 1=여", "DM",
"RACE", "인종", "Integer", "-", "1=아시아인, 2=백인, 3=기타", "DM",
"BWT", "Baseline 체중", "Numeric", "kg", "40-120", "DM",
"DOSE_GRP","용량군", "Numeric", "mg", "5, 10", "EX",
"BSCRD", "Baseline SCORAD", "Numeric", "score", "40-90", "PD",
"CYP2C19", "CYP2C19 대사 표현형", "Integer", "-", "1=EM, 2=IM, 3=PM", "Genomic",
"ALC", "림프구 절대 수 (시간변동)", "Numeric", "cells/μL", "200-4800", "LB",
"BALC", "Baseline 림프구 절대 수", "Numeric", "cells/μL", "1000-4000", "LB"
)
data_spec |>
gt() |>
tab_header(
title = "Tofacitinib PK-PD 통합 데이터셋 사양서",
subtitle = "Data Specification Document"
) |>
cols_label(
Variable = "변수명",
Label = "설명",
Type = "유형",
Unit = "단위",
Values = "값 범위",
Source = "출처"
) |>
tab_style(
style = cell_text(weight = "bold"),
locations = cells_body(columns = Variable)
)12.5 약리학 노트: Tofacitinib 약리학
12.5.1 JAK-STAT 경로와 Tofacitinib의 작용 기전
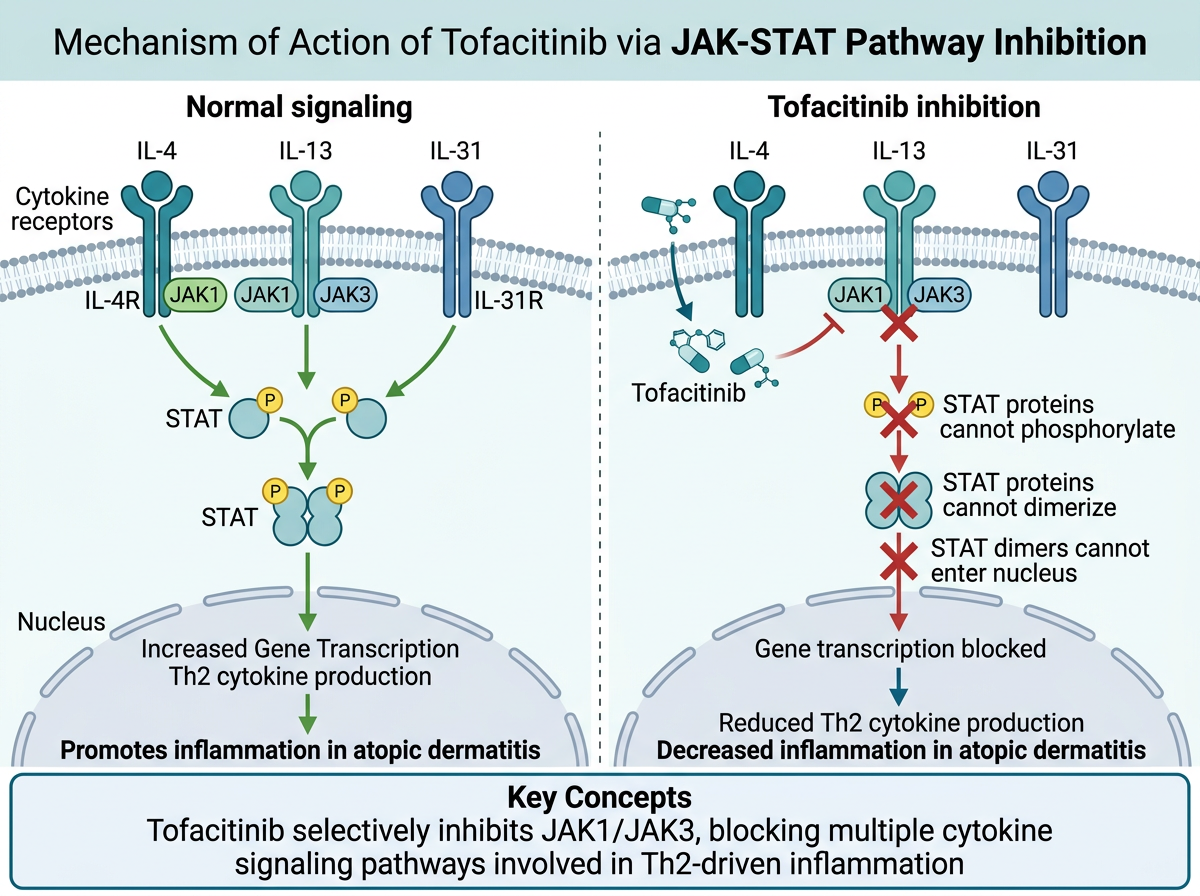
그림 12.3 은 Tofacitinib이 JAK1/3을 억제하여 사이토카인 신호전달을 차단하는 기전을 도식화한 것입니다. JAK-STAT 경로는 다양한 사이토카인과 성장인자의 세포 내 신호전달을 매개하는 핵심 경로입니다. 이 경로의 주요 구성요소는 다음과 같습니다:
- 사이토카인 수용체: 세포 표면에서 사이토카인을 인식
- JAK (Janus Kinase): JAK1, JAK2, JAK3, TYK2 — 수용체에 결합하여 신호를 전달
- STAT (Signal Transducer and Activator of Transcription): 핵으로 이동하여 유전자 발현 조절
Tofacitinib은 JAK1과 JAK3을 선택적으로 억제하는 소분자 약물입니다. JAK1/3 경로를 통해 신호를 전달하는 사이토카인에는 다음이 포함됩니다:
| 사이토카인 | JAK 조합 | 아토피 피부염에서의 역할 |
|---|---|---|
| IL-4 | JAK1/JAK3 | Th2 분화, IgE 생산 증가 |
| IL-13 | JAK1/TYK2 또는 JAK1/JAK2 | 피부 장벽 파괴, 섬유화 |
| IL-31 | JAK1/JAK2 | 가려움증의 주요 매개체 |
| IL-2 | JAK1/JAK3 | T세포 활성화 및 증식 |
| IL-6 | JAK1/JAK2 | 급성기 염증 반응 |
| IL-15 | JAK1/JAK3 | NK세포 및 T세포 항상성 유지 |
| IFN-γ | JAK1/JAK2 | Th1 면역반응, 케라티노사이트 활성화 |
12.5.2 아토피 피부염에서의 치료 효과
Tofacitinib이 아토피 피부염에서 효과를 나타내는 기전:
- 가려움증 억제: IL-31 신호 차단으로 가려움증의 신경 신호 감소. 환자들이 가장 먼저 경험하는 개선 증상
- 피부 염증 억제: IL-4/IL-13 경로 차단으로 Th2 면역반응 감소, 표피 장벽 복구 촉진
- IgE 감소: IL-4 의존적 B세포 class switching 억제로 혈청 IgE 감소
- 피부 장벽 회복: 케라티노사이트의 분화 및 filaggrin 발현 정상화
12.5.3 PK 특성
Tofacitinib의 약동학 파라미터:
| 파라미터 | 값 | 임상적 의미 |
|---|---|---|
| 경구 생체이용률 (F) | ~74% | 높은 흡수율, 음식 영향 없음 |
| Tmax | 0.5-1시간 | 빠른 흡수 |
| t1/2 | ~3시간 | 짧은 반감기 → BID 투약 필요 |
| 단백결합률 | ~40% | 중간 수준 |
| 대사 | CYP3A4 (주), CYP2C19 (부) | 약물 상호작용 주의 |
| 배설 | 간대사 70%, 신배설 30% | 간/신장 장애 시 용량 조절 |
| Vd/F | ~87 L | 넓은 분포 용적 |
| CL/F | ~30 L/hr | 체중 의존적 |
12.5.4 안전성 고려사항
Tofacitinib을 포함한 JAK 억제제의 주요 안전성 우려:
FDA는 2021년 tofacitinib의 안전성 경고를 강화했습니다. ORAL Surveillance 연구 결과를 바탕으로 다음 위험이 확인되었습니다:
- 심각한 감염: 결핵, 기회감염, 대상포진(herpes zoster) — 특히 고령자와 면역 저하 환자에서 위험 증가
- 혈전증: 심부정맥혈전증(DVT)과 폐색전증(PE) 위험 증가
- 악성 종양: 림프종을 포함한 악성 종양 위험 증가
- 주요 심혈관 이벤트(MACE): 심근경색, 뇌졸중 위험 증가
- 림프구감소증: 용량 의존적 림프구 감소 → ALC < 500 cells/μL 시 투약 중단
이러한 안전성 프로파일은 PK-PD 분석에서 노출-안전성(exposure-safety) 관계 분석의 필요성을 강조합니다. 특히 림프구 수 감소는 약물 노출과 직접적으로 연관되므로, PK-PD 모델링의 주요 대상입니다.
12.5.5 SCORAD (SCORing Atopic Dermatitis)
SCORAD는 아토피 피부염의 중증도를 평가하는 복합 점수 시스템입니다:
\[ \text{SCORAD} = \frac{A}{5} + \frac{7B}{2} + C \]
여기서:
- A: 병변 범위 (Extent, 0-100%) — Rule of Nines 방법
- B: 강도 (Intensity, 0-18) — 6개 항목 × 0-3점 (홍반, 부종, 삼출, 태선화, 건조, 찰상)
- C: 자각 증상 (Subjective symptoms, 0-20) — 가려움증 + 수면장애 (각 0-10 VAS)
중증도 분류:
| SCORAD | 중증도 |
|---|---|
| < 25 | 경증 (Mild) |
| 25-50 | 중등도 (Moderate) |
| > 50 | 중증 (Severe) |
12.6 Claude Code 활용 팁
12.6.1 복잡한 데이터 병합 요청
PK-PD 데이터셋 구축에서 가장 시간이 많이 소요되는 단계는 여러 소스의 데이터를 병합하는 과정입니다. Claude Code에 다음과 같이 요청할 수 있습니다:
"다음 세 가지 데이터 소스를 NONMEM PK-PD 형식으로 병합해주세요:
1. dosing.csv: USUBJID, EXSTDTC, EXDOSE, EXROUTE 컬럼
2. pk_concentrations.csv: USUBJID, PCDTC, PCSTRESN 컬럼
3. scorad_scores.csv: USUBJID, VISITNUM, SCORAD_TOTAL 컬럼
요구사항:
- CMT: 1(투약), 2(PK), 3(PD)
- TIME: 첫 투약 기준 시간(hour) 단위
- DVID: 1(PK), 2(PD)
- LOCF로 공변량 처리
- 데이터 검증 함수도 작성
- 데이터 사양서 테이블 생성"12.6.2 검증 체크리스트 자동 생성
"이 PK-PD 데이터셋의 포괄적인 검증 체크리스트를 R 코드로 구현해주세요:
1. 필수 컬럼 존재 확인
2. EVID/MDV/CMT/DVID 일관성
3. TIME 순서 확인
4. 공변량 결측 패턴
5. PK/PD 레코드 수 대상자별 요약
6. 이상값 탐지 (PK: 3 SD 초과, PD: 범위 이탈)
7. 결과를 gt 테이블과 플래그 리스트로 출력"데이터 병합을 요청할 때는 다음 정보를 반드시 포함하세요:
- 각 데이터 소스의 컬럼명과 유형 — 정확한 컬럼명을 제공
- 병합 키(key) — 어떤 변수로 데이터를 연결하는지
- 시간 형식 — ISO 8601, POSIX, 상대시간 등
- 단위 — 농도, 용량, 시간의 단위
- 결측 처리 방법 — LOCF, 보간, 제외 등
12.7 연습 문제
12.7.1 확인 문제
PK-PD 통합 데이터셋에서 CMT=1, CMT=2, CMT=3이 각각 의미하는 바를 설명하고, 각 CMT에 대응하는 EVID와 MDV 값의 일반적인 조합을 기술하세요.
DVID와 CMT의 차이점을 설명하세요. 왜 두 변수가 모두 필요합니까?
PK 데이터의 DV(ng/mL)와 PD 데이터의 DV(SCORAD score)가 하나의 DV 컬럼에 혼재할 때, 이 스케일 차이를 처리하는 세 가지 방법을 설명하세요.
LOCF(Last Observation Carried Forward)와 선형 보간의 장단점을 비교하고, 림프구 수(ALC) 공변량에 대해 어떤 방법이 더 적절한지 근거를 들어 설명하세요.
Tofacitinib의 반감기가 약 3시간인데 BID(12시간 간격)로 투약하는 이유를 약력학적 관점에서 설명하세요. (힌트: PK-PD disconnect 개념)
12.7.2 R 과제
다중 PD 엔드포인트 데이터셋 구축: 이 장의 Tofacitinib 데이터에 가려움증 NRS(0-10) 엔드포인트를 추가하여, CMT=5/DVID=4인 레코드를 포함하는 확장된 PK-PD 데이터셋을 구축하세요. NRS는 baseline 6-9, 12주 후 2-5 범위로 시뮬레이션하세요.
시간 변동 공변량 비교 분석: ALC 데이터에 대해 LOCF와 선형 보간을 각각 적용하고, 두 방법의 결과를 비교하는 그래프를 만드세요. 대상자 3명을 선택하여 time-course plot을 생성하세요.
데이터 검증 보고서:
validate_pkpd_dataset()함수를 확장하여, 다음 검증 항목을 추가하고 gt 테이블로 결과를 출력하세요:- PK 관측값의 이상값 탐지 (평균 ± 3SD 기준)
- PD 관측값의 범위 확인 (SCORAD: 0-103)
- 대상자별 PK/PD 관측 수 불균형 확인
- 공변량의 생리학적 범위 확인 (예: 체중 30-150kg, ALC 200-10000)
12.7.3 Claude Code 과제
Claude Code에 다음과 같이 요청하세요: > “Tofacitinib PK-PD 데이터셋을 검증하는 종합 보고서를 Quarto 문서로 만들어줘. 데이터 구조 요약, 대상자별 레코드 수 히트맵, 공변량 분포 플롯, 시간 변동 공변량의 time-course, PK-PD 레코드의 시간 정렬 확인 그래프를 포함해줘. 모든 코드는 함수화하고, 재사용 가능하게 구조화해줘.”
Claude Code의 출력을 검토하고, 데이터 검증에서 발견된 문제가 있다면 수정하세요.